氨基酸是一种含有碱性氨基和酸性羧基的有机化合物,是构成动物营养所需蛋白质的基本物质。氨基酸呈无色晶体状,一般易溶于水、酸溶液和碱溶液中,不溶或微溶于乙醇或乙醚等有机溶剂,其熔点超过200℃,比一般有机化合物的熔点高很多。由于氨基酸分子中同时含有酸性基团和碱性基团,所以氨基酸既能和较强的酸反应,也能与较强的碱反应而生成稳定的盐,具有两性化合物的特征。
氨基酸的亲疏水性指的是氨基酸的化学特性,主要由其侧链基团(R基团)决定。
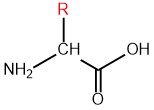
亲水基团所占的体积越多,亲水性就越强,反之,疏水性也一样。
亲水基团包含有:羧基、磺酸基、硫酸基、磷酸基、氨基、季铵基、含氧基团、醚基、羟基。其余的基本都是疏水基团。
氨基酸,是羧酸碳原子上的氢原子被氨基取代后的化合物,氨基酸分子中含有氨基和羧基两种官能团。与羟基酸类似,氨基酸可按照氨基连在碳链上的不同位置而分为α-,β-,γ-...w-氨基酸,但经蛋白质水解后得到的氨基酸都是α-氨基酸,而且只有二十几种,是构成蛋白质的基本单位。
极性和非极性这两个概念经常和疏水亲水联系在一起。
根据相似相容原理,极性溶质溶于极性溶剂中,非极性溶质溶于非极性溶剂中。水经常作为溶剂,是极性的,所以极性氨基酸可看作是易溶于水的氨基酸,反之则是不易溶于水。
另一方面,也可以从氨基酸结构来看,氨基酸的性质主要取决于侧链基团R,如果R只是H或是C、H两元素组成的话,都是疏水的,如果含有极性侧链基团,如-OH、-SH、-COOH、-NH2等,那么这个氨基酸就是极性的。
一般来说,亲水和疏水相互联系,例如大部分蛋白质表面都是极性氨基酸,内部为非极性氨基酸,所以一般情况下这些蛋白质是溶于水的,但是当蛋白质变性后,内部的非极性氨基酸暴露出来,此时蛋白质就变为沉淀了。
组成蛋白质的疏水性最强的氨基酸是异亮氨酸(ILE),极性最强的氨基酸是精氨酸(Arg)。
非电离极性侧链氨基酸:丝氨酸(Ser)、苏氨酸(Thr)、酪氨酸(Tyr)、半胱氨酸(Cys)、天冬酰胺(Asn)、谷氨酰胺(Gln)
酸性侧链氨基酸:谷氨酸(Glu)、天冬氨酸(Asp)、赖氨酸(Lys)
碱性侧链氨基酸:精氨酸(Arg)、组氨酸(His)
如有侵权内容,请联系本公司工作人员删除文章。